登録販売者試験の解説とポイントを過去問題にフォーカスして記載していきます。
厚生労働省の試験問題作成の手引きを基に分かり易い内容に変えて解説しています。
実際の過去問題から作成したポイントテストもありますので、是非解いて見てくださいね。
独学で学ばれている方も問題なく解けることが実感できるかと思います。

第1章:医薬品に共通する特性と基本的な知識
問題概要:
1章からの出題が120問中20問を占めますが、厚生労働省による「試験問題の作成に関する手引き(平成30年3月)」では約400ページ中、わずか18ページです。
また、問題のレベルも全体と比べ優しく作られていることが多いです。つまり、効率よく得点を取れる章となってますので、第1章でしっかり得点を取っていきまよう。
(問題作成の手引きにて第一章のポイントが記載されています。覚える必要はありませんが一読しておきましょう。)
問題作成のポイント
○ 医薬品の本質、効き目や安全性に影響を与える要因等について理解していること
○ 購入者等から医薬品を使用しても症状が改善しないなどの相談があった場合には、医療機 関の受診を勧奨するなど、適切な助言を行うことができること
○ 薬害の歴史を理解し、医薬品の本質等を踏まえた適切な販売等に努めることができること
(引用:試験問題の作成に関する手引き|厚生労働省)
1)医薬品の本質
医薬品とは
1.生命関連製品であり、有用性が認められたもの
医薬品は多くの場合、人体に取り込まれて作用し、効果を発現するものです。
人の疾病の診断、治療若しくは予防に使用されること、または人の身体の構造や機能に影響を及ぼすことを目的とする生命関連製品であり、その有用性が認められたものです。
2. 好ましくない反応を生じる場合がある
医薬品も人体にとっては異物(外来物)であり、作用のすべてが解明されているわけではないため好ましくない反応(副作用)を生じる場合があります。
人体に使用しない医薬品(殺虫剤や検査に使用する医薬品など)でも人の健康に影響を与える場合があります。
たとえば、
- 殺虫剤の中には誤って人体に使用すると健康を害するものがある。
- 検査薬は検査結果について正しい解釈や判断がなされなければ医療機関を受診して適切な治療を受ける機会を失うおそれがある。
3. 適正な使用が図られる必要がある
医薬品は科学的な根拠に基づく適切な理解や判断によって適正な使用が図られる必要があります。医薬品は、その効能効果、用法用量、副作用などの必要な情報が適切に伝達され購入者などが適正に使用するで、はじめてその役割を十分に発揮します。
4. 市販後にも有効性や安全性の確認がされる
医薬品は市販後にも有効性、安全性などの確認が行われており、新たな知見や使用成績の結果などを踏まえ、リスク区分の見直し、承認基準の見直しなどがなされ、販売時の取扱い、製品の成分分量、効能効果、用法用量、使用上の注意などが変更となった場合には、添付文書や製品表示の記載に随時反映されています。

製品表示:製品の外箱などに記載されている事項
5. 高い水準で均一な品質が保証されていなければならない
医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律に基づき、健康被害の発生の可能性の有無にかかわらず、異物の混入、変質などがある医薬品を販売してはなりません。
また一般用医薬品として販売される製品は、製造物責任法(PL法)の対象でもあります。
PL法は、製造物の欠陥により、人の生命、身体、財産に係る被害が生じた場合における製造業者等の損害賠償の責任について定めており、販売した一般用医薬品に明らかな欠陥があった場合などは、PL法の対象になりえます。
一般用医薬品とは
医薬品には医療用医薬品と一般用医薬品などがあり、いずれも副作用や健康被害のリスクがあります。
医療用医薬品:医師の処方箋や指示により使用する医薬品
一般用医薬品:一般の生活者が自分で選択して使用する医薬品
医療用医薬品と比較して健康被害など保健衛生上のリスクが相対的に低い一般用医薬品においても、人の健康に影響を与えるおそれがあります。
一般用医薬品には、添付文書や製品表示に必要な情報が記載されていますが、一般の生活者が選択して使用するため、誤解や認識不足を生じることがあります。
そのため、販売に専門家が関与し、専門用語を分かりやすい表現で伝えるなどの適切な情報提供を行い、購入者が知りたい情報を十分に得ることができるよう相談に対応することが不可欠です。
医薬品の販売などを行う者は、随分更新される新しい情報の把握に努めるとともに、製品回収などの措置がなされることもあるので、製造販売業者等からの情報に日頃から留意しておくことが重要です。
ポイントテスト1
下記問題の正誤を求めよ(回答は下)
(1)医薬品が人体に及ぼす作用は複雑、多岐に渡り、そのすべては解明されていない。
(2)人体に対して使用されない医薬品は、健康を害するおそれがある。
(3)検査薬については、健康を害するおそれがない。
(4)医薬品は、人の疾病の診断、治療に使用されるが、予防は含まない。
(5)医薬品は、有効性、安全性等に関する情報が集積されており、一定期間ごと新たな情報が付加されるものである。
解答と解説
ポイントテスト1
(1)〇
(2)〇
(3)× :検査薬も健康を害する可能性がある
(4)× :医薬品は予防にも使用される
(5)× :医薬品の情報は随時、新たな情報が付加される
2)医薬品のリスク評価
医薬品の効果とリスクは、用量と作用強度の関係(用量-反応関係)に基づいて評価されます。
医薬品の用量反応関係とは
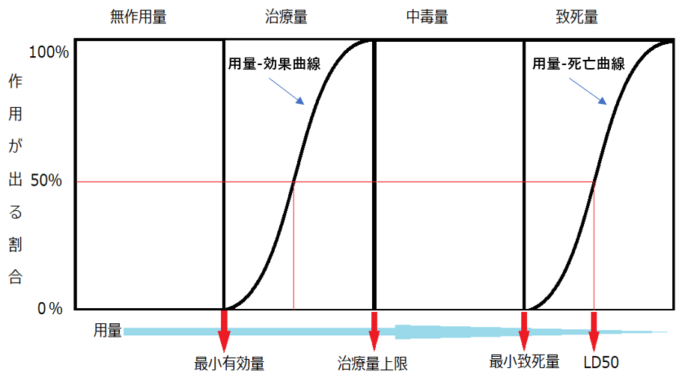
薬物用量の増加に伴い、次の順番で効果や毒性が発現します。
- 無作用量 :効果が発現しない用量
- 最小有効量 :治療効果が表れる最小用量
- 治療量 :作用が発現するが、毒性は少ない量
- 治療量上限 :この量を超えても、作用が増強しない量
- 中毒量 :効果よりも有害反応が強く発現する量
- 最小致死量 :死亡する最小量
- 致死量 :死に至る量
動物実験により求められる50%致死量(LD50)は、薬物の毒性の指標として用いられます。

医薬品は、少量の投与でも長期投与されれば慢性的な毒性が発現する場合があります。また、発がん作用、胎児毒性や組織・臓器の機能不全を生じる場合もあります。
医薬品開発の基準
医薬品には、食品などよりもはるかに厳しい安全性基準が要求されており、医薬品開発の国際的な標準化(ハーモナイゼーション)制定の流れの中で次の基準が設けられています。

1.Good Laboratory Practice
(GLP)
医薬品の安全性に関する非臨床試験の基準。
(補足)
医薬品のリスク評価はGLPのほかに、「医薬品毒性試験法ガイドライン」に沿って、単回投与毒性試験、反復投与毒性試験、生殖・発生毒性試験、遺伝毒性試験、がん原性試験、依存性試験、抗原性試験、局所刺激性試験、皮膚感作性試験、皮膚光感作性試験などの毒性試験が厳格に実施されています。
2.Good Clinical Practice
(GCP)
ヒトを対象とした臨床試験の実施の基準。これに準拠した手順で安全な治療量を設定することが新規医薬品の開発に関連する臨床試験(治験)の目標の一つである。
3.Good Post-marketing Study Practice
(GPSP)
医薬品に対しての製造販売後の調査及び試験の実施の基準。
4.Good Vigilance Practice
(GVP)
医薬品に対しての製造販売後安全管理の基準。
GPSPとGVPの違いって何?
GPSPは、「市販前には調査出来なかった、高齢者、小児について、もしくは併用薬についてはどうか?」等を調査するための基準
GVPは、製造販売後における安全管理に関しての情報収集や市販直後調査の手順書等に関しての基準
=「どうやって安全性について収集、管理し、情報発信していくか」に関する基準
ポイントテスト2
下記問題の正誤を求めよ(回答は下)
(1)医薬品の効果とリスクは、用量と作用強度の関係(用量-反応関係)に基づいて評価される。
(2)少量の投与であれば、長期投与されても慢性的な毒性が発現することはない。
(3)医薬品は、市販後にも、医学・薬学等の新たな知見、使用成績等に基づき、その有効性、安全性等の確認が行われる仕組みになっている。
(4)投与量と効果又は毒性の関係は、薬物用量を増加させるに伴い、「治療量」から「無作用量」に至り、無作用量上限を超えると、「中毒量」、「最小致死量」を経て、「致死量」に至る。
(5)医薬品の製造販売後安全管理の基準として、Good Post-marketing Study Practice(GPSP)が制定されている。
回答と解説
ポイントテスト2
(1)〇
(2)× :少量でも長期投与されれば、毒性が発現する可能性がある
(3)〇
(4)× :「無作用量」から「治療量」に至り、治療量上限を超えると、「中毒量」、「最小致死量」を経て「致死量」に至る
(5)× :GPSPではなくGVP
3)健康食品
健康増進や維持の助けとなることが期待されるいわゆる「健康食品」はあくまで食品であり、医薬品とは法律上区別されます。
しかしながら、国が示す要件を満たした下表の食品に関しては保健機能や用途を記載することができます。

| 消費者庁 | 表示内容 | 内容例 | |
| 特別用途食品 | 許可等のマーク付き※1 | 特別な用途 | えん下困難者用 、乳児用等 |
| 特定保健用食品 | 許可等のマーク付き※2 | 特定の保健の用途 | 血圧が高めの方に適する等 |
| 栄養機能食品 | 個別審査なし | ビタミン・ミネラルなどの栄養成分の機能 | 鉄は、赤血球を作るのに必要な栄養素である等 |
| 機能性表示食品(注) | 個別審査なし(届出制) | 科学的根拠に基づいた機能 | 脂肪の吸収を抑える等 |
(注)機能性表示食品は、疾病に罹患していない(=かかっていない)者の健康維持及び増進に役立つ機能(疾病リスクの低減に係るものを除く)を表示するものです。
 いわゆる健康食品は、カプセル、錠剤等の医薬品と類似した形状で販売されているものも多く、誤った使用法や個々の体質により健康被害を生じた例も報告されています。
いわゆる健康食品は、カプセル、錠剤等の医薬品と類似した形状で販売されているものも多く、誤った使用法や個々の体質により健康被害を生じた例も報告されています。
また医薬品との相互作用で薬物治療の妨げになることもあります。
そのため、医薬品を扱う者は、いわゆる健康食品は法的にも、また安全性や効果を担保する科学的データの面でも医薬品とは異なるものであることを認識し、消費者に指導・説明を行わなくてはなりません。
4)セルフメディケーションへの積極的な貢献
持続可能な医療制度の構築に向け、医療費の増加や国民負担の増大を解決し、健康寿命を伸ばすことが日本の大きな課題です。地域住民の健康相談への対応や、一般用医薬品の販売、医療機関の受診を勧める業務は、セルフメディケーションの推進に欠かせません。
セルフメディケーションとは:世界保健機関(WHO)によれば、「自分自身の健康に責任を持ち、軽度な身体の不調は自分で手当てすること」をいう。
一般用医薬品の販売等を行う登録販売者は、一般用医薬品等に関する正確で最新の知識を常に修得するよう心がけるとともに、薬剤師や医師、看護師などの医療スタッフや行政などとも連携して、地域住民の健康維持・増進、生活の質(QOL)の改善・向上などに携わることが望まれます。
また、適切な健康管理の下で医療用医薬品からの代替を進める観点から、条件を満たした場合にスイッチOTC医薬品の購入の対価について、一定の金額をその年分の総所得金額等から控除するセルフメディケーション税制が導入されました。
令和4年1月の見直しにより、スイッチOTC医薬品以外にも腰痛や肩こり、風邪やアレルギーの諸症状に対応する一般用医薬品が税制の対象となります。

ポイントテスト3
下記問題の正誤を求めよ(回答は下)
(1)いわゆる健康食品の中にはカプセル、錠剤等の医薬品と類似した形状で発売されているものも多いが、誤った使用法により健康被害を生じた例は報告されていない。
(2) 医薬品を扱う者は、いわゆる健康食品は法的にも、また安全性や効果を担保する科学的データの面でも医薬品とは異なるものであることを認識し、消費者に指導・説明を行わなくてはならない。
(3)「機能性表示食品」は、疾病に罹患している者の健康の維持及び増進に役立つ機能を表示するものである。
(4)栄養機能食品は、各種ビタミン、ミネラルに対して栄養成分の健康機能の表示をすることができる。
(5)スイッチOTC医薬品以外の風邪の諸症状に対する一般用医薬品はセルフメディケーション税制の対象にならない。
解答と解説
ポイントテスト3
(1)× :健康被害が生じた報告がある
(2)〇
(3)× :疾患にり患している者ではなく、罹患していない者。
(4)〇
(5)× :セルフメディケーション税制の対象になる。


